La industria farmacéutica nos está abandonando
Artículo basado en el libro: "Superbacterias" de José Ramos Vivas.
8 min read


Cáncer. Tumor. Metástasis. Estas son palabras que, puesta en la boca de tu médico de cabecera, hacen que se te hiele la sangre. En otro artículo ya analizamos los entresijos de las enfermedades englobadas como cáncer, y si lo leíste, seguro que recuerdas que la posibilidad de desarrollar cáncer aumenta con la edad. Además, muchos tipos de cáncer están favorecidos por factores ambientales como el tabaco, la contaminación, el sol o la dieta. Algunos son hereditarios, otros son contraídos por bacterias o por virus, pero hay algo omnipresente asociado a este conjunto de enfermedades: su enorme diversidad. Por suerte, hay muchos y muy buenos grupos de científicos por todo el mundo buscando un tratamiento o un medicamento contra esta patología. Decenas de miles de estudiantes realizan sus tesis doctorales sobre algún aspecto del cáncer y miles de millones de euros son invertidos en estas investigaciones. Se han realizado innumerables ensayos clínicos y experimentado con millones de moléculas para conseguir nuevos tratamientos. El cáncer es complejo y caro, y las farmacéuticas lo saben. De hecho, la principal razón por la que las empresas farmacéuticas se interesan por el cáncer es porque sus tratamientos son caros. El número de tipos de cáncer es muy elevado y el número de personas que padecerán esta enfermedad a lo largo de su vida es muy alto. El cáncer es una maldición para la mayoría, pero es un negocio para las farmacéuticas. Sin embargo, la OMS (Organización Mundial de la Salud) ya nos advirtió hace unos años de que para 2050, morirá más gente por culpa de bacterias resistentes a los antibióticos que por culpa del cáncer. En concreto, en 2050, cada 3 segundos morirá una persona por bacterias resistentes a los antibióticos y cada 4 segundos morirá una persona por cáncer. Es decir, mientras que el cáncer matará en unos años a unas 8,2 millones de personas anualmente, las superbacterias resistentes a los antibióticos acabarán con la vida de 10 millones cada año. Entonces, ¿las farmacéuticas también están invirtiendo tanto en el desarrollo de antibióticos? No, de hecho, están haciendo lo contrario.
Las empresas farmacéuticas están abandonando muchos de sus programas de investigación y desarrollo de nuevos antibióticos, y la gran mayoría de nosotros no lo sabe. Incluso muchos médicos ignoran que hace más de 30 años que no aparecen antibióticos revolucionarios en el mercado, y tampoco aparecerán en un futuro cercano. Los sanitarios siguen recetando los que ya conocen como si su efectividad no estuviera desapareciendo. Y esto es un error, ya que los antibióticos son el único medicamento cuyo mal uso no solo puede afectar al paciente, sino que puede terminar afectando a toda la sociedad. Como la población mundial no hace más que crecer y cada vez hay más viajes, más catástrofes naturales, más desplazamientos de grupos de gente, las enfermedades infecciosas también están aumentando. En esta tesitura, los antibióticos deberían representar un negocio redondo ¿no? Pues la verdad es que no. Los antibióticos ya no son rentables, han muerto de su propio éxito. Si alguna vez los has tomado, te habrás dado cuenta de que solo son necesarios en un periodo corto de tiempo y que son muy baratos. El cáncer, por el contrario, tiene tratamientos muy caros y muy largos. No es que las farmacéuticas hayan reducido su gasto en I+D, pero el dinero se destina ahora a medicamentos más rentables. Según la Asociación Americana de Enfermedades Infecciosas, en los años 80, había 30 potentes compañías farmacéuticas investigando en la búsqueda y desarrollo de nuevos antibióticos. En el año 2011 solo quedaban 5, y para 2019 ese número se redujo a 3. Gigantes de la industria como Novartis, ahora buscan compradores para sus más de 30 proyectos a medio terminar sobre antibióticos.
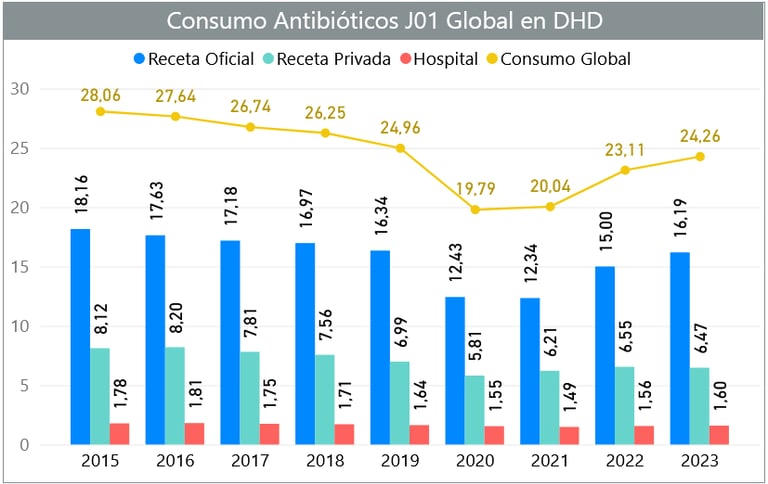
Evolución del consumo global de antibióticos (Fuente: PRAN)
Por supuesto, muchos laboratorios de todo el mundo (sobre todo públicos) realizan investigación básica para el desarrollo de nuevos antibióticos. Pero tras los estudios iniciales, es necesario purificar y producir una cantidad suficiente de un compuesto para pasar a los ensayos de seguridad y toxicidad en células animales. Luego se estudia su absorción por el cuerpo, si dejan residuos, si son equivalentes o mejores que otro compuesto existente en el mercado, cuál es la mejor vía de administración, cuál es la mejor dosis… Posteriormente se realizan ensayos en voluntarios y pacientes y se comprueba si son efectivos y seguros. Toda esta información es minuciosamente revisada por la Agencia Europea del Medicamento, la FDA o la autoridad correspondiente. Todo este proceso lleva años y se estima que de cada 10.000 moléculas que se estudian en investigación básica, tras unos 10 años de ensayos y millones de euros de inversión, solo 1 podrá verse en las farmacias. Es un proceso que los laboratorios pequeños no pueden costear, ni siquiera muchos Gobiernos tienen esa capacidad. Este esfuerzo, que de media tarda unos 10 años con el gasto de unos 800 millones de euros de media, solo pueden costearlo las grandes farmacéuticas. Sin embargo, el objetivo de estas grandes compañías es ganar dinero, y hay multitud de enfermedades que son mucho más rentables. Y no solo enfermedades como el cáncer, sino que otras enfermedades infecciosas también son muy rentables, todo depende del tratamiento. Por ejemplo, el sida, que es producido por un virus y no por una bacteria. Mientras que los enfermos de sida deben consumir antirretrovirales por el resto de su vida, el tratamiento medio con antibióticos dura entre 5 y 10 días. Además, el sida suele ser una enfermedad que se adquiere a una edad temprana (antes de los 30 años), lo que alarga el tratamiento del enfermo por décadas y engrosa los bolsillos de las farmacéuticas. En el año 2007, un equipo de investigadores norteamericanos publicó un estudio en el que se observaba que el número de antirretrovirales contra el VIH aprobados por la FDA para su uso en humanos, era ya mayor que el número de antibióticos aprobados para hacer frente a las todas las enfermedades junta causadas por bacterias.
Para las empresas farmacéuticas hay muchas otras patologías más rentables que las causadas por las bacterias. La hipertensión, la disfunción eréctil, la depresión, la diabetes, la obesidad… Enfermedades que aparecen en personas no muy jóvenes pero que pueden durar el resto de su vida. Todos conocemos a alguien con problemas de tensión que toma sintrom diariamente. Estos medicamentos no curan la enfermedad, tan solo alivian los síntomas, por lo que tienen que seguir tomándolos y comparándolos, y las farmacéuticas haciendo dinero. Muchos diabéticos tienen que regular su ingesta de azúcar y medicarse el resto de su vida, y las farmacéuticas haciendo dinero. Muchos adultos que quieren seguir disfrutando del sexo deben tomar la famosa pastilla azul y deben tomarla cada ve que lo práctican, y las farmaceúticas haciendo dinero. Los beneficios con estas patologías son eternos, pero con los antibióticos no. Además, otros de los factores que desaniman a las farmacéuticas a desarrollar antibióticos son las políticas de control y reducción de uso de estos medicamentos. Y es que hay datos que indican que los países que menos antibióticos recetan, son los que lo hacen de manera más adecuada, los que emplean el menor número de antibióticos de amplio espectro y los que menor porcentaje de bacterias resistentes tienen. Es decir, utilizar de forma más racional los antibióticos, es el mejor método para reducir la aparición de bacterias resistentes que amenazan al mundo. Pero claro, utilizarlos mejor, implica utilizar menos y que los hospitales reduzcan sus compras de los mismos, ¿Quien quiere producir un medicamento que cada vez se compra menos?
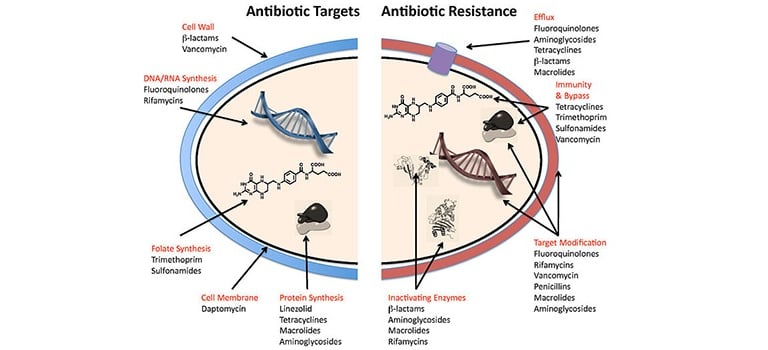
Dianas de los antibióticos y mecanismos de resistencia bacteriana (Fuente: Dañocerebral)
Otro de los problemas de la investigación de antibióticos para las farmacéuticas se basa en la pérdida de eficacia que presentan estos medicamentos. Aunque suene terrible, las bacterias han desarrollado resistencia frente a todos, absolutamente todos los antibióticos que disponemos. De hecho, ya se ha acuñado el término bacteria "panresistente", que son aquellas que han adquirido resistencia a todos los antibióticos de nuestras farmacias. Cuando hay muchas bacterias resistentes a un antibiótico este ya no es eficaz, y hay que dejar de venderlo, y por lo tanto, de producirlo. La penicilina se descubrió en 1928, pero no comenzó a aplicarse hasta 1941, tan sólo un año después ya se aislaron cepas de Staphylococcus aureus resistentes a este antibiótico. Las tetraciclinas se descubrieron en 1945, para 1953 ya se identificaron bacterias resistentes. Los macrólidos aguantaron 1 año, de 1952 a 1953. Las quinolonas se descubrieron en 1962 y las bacterias resistentes aparecieron en 1966. En 1973 aparecieron cepas resistentes a la fosfomicina, descubierta en 1969. Los antibióticos monobactámicos aparecieron en 1979 y la primera cepas resistentes en 1981. Sin embargo, hay algunos casos en los que las bacterias lo tuvieron más difícil como las cefalosporinas, descubiertas en 1948, mientras que las bacterias resistentes aparecieron en 1966. Los glicopéptidos aguantaron desde 1953 hasta 1986 y los lipopéptidos desde 1987 hasta 2005. Los números varían pero la evidencia demuestra que tarde o temprano las bacterias hallan un mecanismo para hacer frente a cada antibiótico que descubrimos ¿Quién va invertir 10 años de esfuerzo y 800 millones de euros en el desarrollo de un fármaco que deja de ser útil en 2 años? Lógicamente, nadie cuyo objetivo principal sea el beneficio económico.
El último de los problemas al que se enfrenta la industria farmacéutica a la hora de desarrollar nuevos antibióticos es un viejo conocido de todos, la burocracia. Son necesarios muchos permisos y la legislación de cada país es diferente y emplea reglas distintas para poner un medicamento en circulación. Por ejemplo, hace más de 20 años, la FDA requería estudios de no-inferioridad de un fármaco; es decir, que las tasas de curación de ese nuevo fármaco no debían ser menores del 10% respecto a un antibiótico similar que ya estuviese en el mercado. Según la revista Nature Biotechnology, esto hizo que empresas como Cubist o Wyeth tuvieran muchos problemas a la hora de sacar a la venta sus respectivos antibióticos. Luego, de la noche a la mañana, la FDA empezó a exigir ensayos controlados con placebo para algunas enfermedades infecciosas. A partir de 2006, la FDA empezó a pedir cohortes más grandes de pacientes (y más costosas) para los estudios de no inferioridad, pasando en algunos casos de los 4.000 pacientes a 8.000, haciendo que varias compañías pasaran de EE.UU. y se mudaran a Europa. Esto hace mucho menos atractiva la investigación en antibióticos en el país norteamericano. Por suerte y por desgracia, estamos en un punto en el que la legislación y la regulación van a tener que cambiar sí o sí para acelerar el proceso de autorización de nuevos antibióticos. En un futuro no muy lejano, las omnipresentes bacterias resistentes no esperarán todas estas trabas burocráticas par acabar con nuestras vidas.
Artículo basado en:






